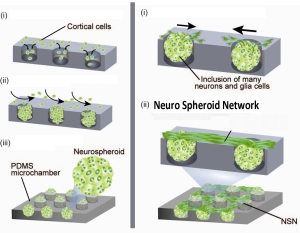
培養神経ネットワーク
ヒト脳内の神経細胞は約860億個に及ぶと言われており、神経細胞同士がシナプスで接続することで、複雑な神経ネットワークを形成する。神経細胞の細胞体の大きさは、およそ0.1mm~0.005mmで、多数の神経突起(軸索・樹状突起)を有している。神経細胞は、培養することでランダムに接続された神経ネットワークを構築することが、昔から報告されてきた。近年、脳内のメカニズム解明や脳疾患治療を目指した生体模倣タイプの神経ネットワークの構築、人工知能開発を目指した神経ネットワークの構築、電子回路として機能させるための神経回路チップの開発などにおいて、人為的にデザインされた神経ネットワーク構築が期待されている。
竹内研究室では、神経細胞を部品のように取り扱うことで、人為的に神経ネットワークをデザインする技術の開発を行っている。これまでにマイクロプレートを利用することで、神経細胞1つ1つを丁寧に配置し神経ネットワークの形状をコントロールする技術、数十個以上の神経細胞を1つのユニットとして取り扱うことで、ユニット同士の接続から形成される神経ネットワークを作製する技術などを開発している。
マイクロプレートによる神経ネットワークの形成
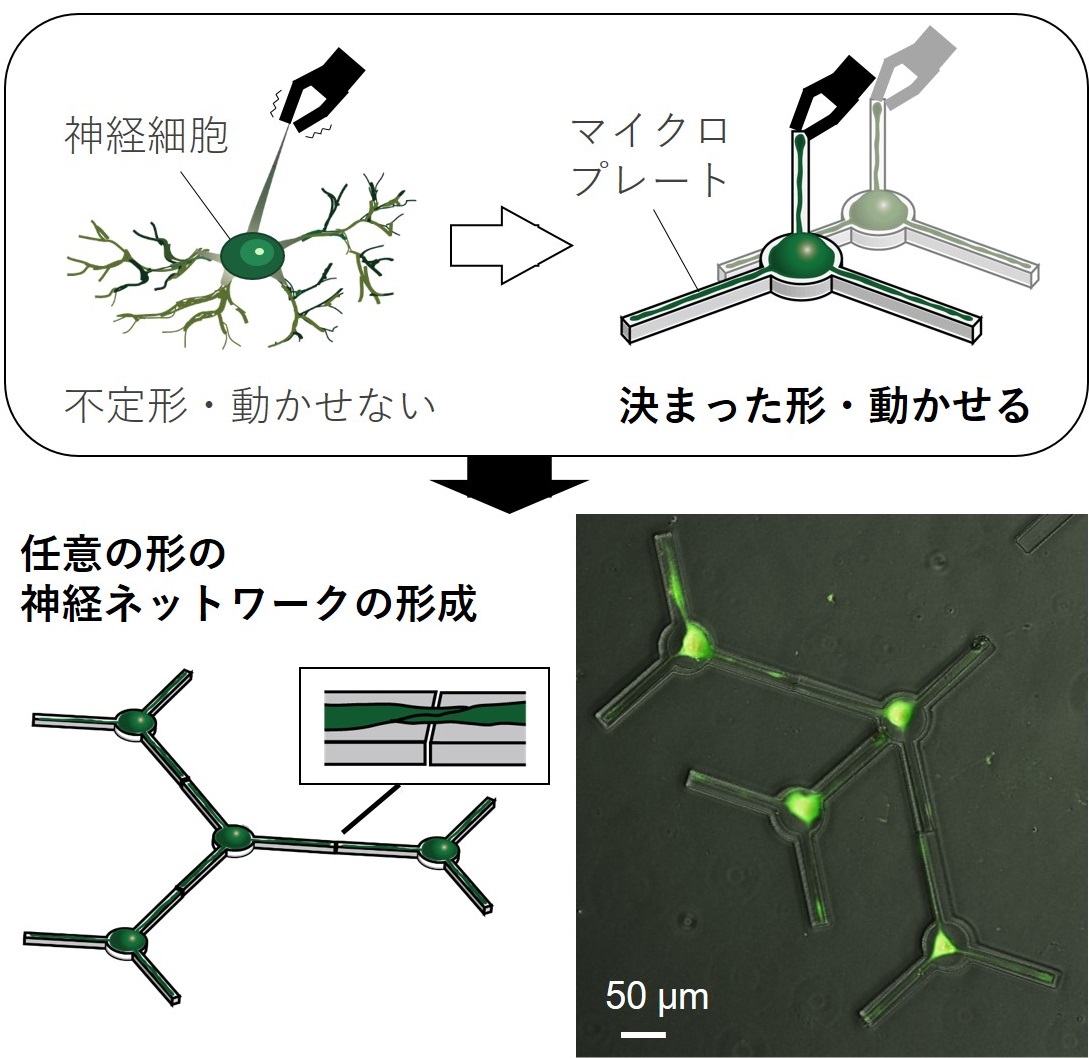
神経細胞は細胞体と多数の神経突起(軸索・樹状突起)を持ち、お互いがつながりネットワークを作ることで、自律思考・創発といった人工物では実現できていない高度な知的情報処理を行っている。神経細胞を操作してこの神経ネットワークを人為的に設計・構築することができれば、電子回路やコンピュータを作るように、自律的に思考する新しい情報処理システム:バイオプロセッサーを構築できるようになるかもしれない。しかしながら、神経細胞の突起は本数や長さなどが不定であり、また人為的に移動させると死んでしまうために、神経細胞を操作して望みの形を持つネットワークを形成することは困難であった。そこで、我々はマイクロ加工技術を駆使して開発したデバイス:マイクロプレートによって、神経細胞の突起の本数や長さを決め、かつ移動させることを可能にした。このデバイスを使えば、神経細胞一つ一つを規格化された電子部品のように取り扱い、それらを自在に移動させて任意の形の神経ネットワークを形成することができる。隣接した神経細胞の間に機能的な接続(シナプス)が形成され、情報伝達が起こることも確認できた。どのような種類の細胞をどのようにつなげれば知的な情報処理が生まれるのかを、作りながら理解する神経科学の実験ツールとして有用であるとともに、人工物を超えたバイオプロセッサーの実現に役立つデバイスであると考えている。
S. Yoshida, et al.: Advanced Healthcare Materials, 2016.
S. Yoshida, et al.: Micromachines, 2018.
神経ブロックを用いたヘテロ3次元神経組織(神経ブロック)形成
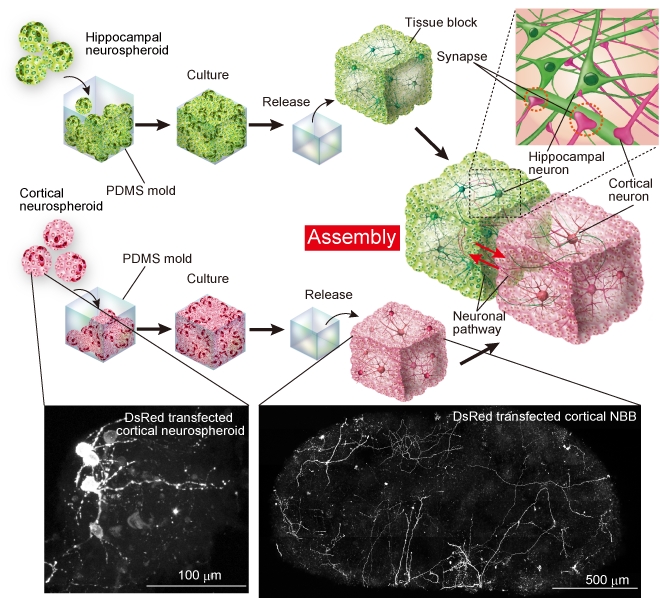
これまで、異なる特定の神経領域間たとえば大脳組織と海馬組織の神経細胞の相互作用をin vitroで観察するためには、神経細胞の2次元共培養技術が主に利用されてきた。しかし2次元共培養法には、生体内で観察されるような3次元空間内部への神経細胞の突起伸展と、生体内に近いより複雑な神経回路を形成する事が難しいという課題が存在した。 我々は、初代培養神経細胞で形成される神経細胞の塊(神経細胞塊)を用いてミリメートルサイズの神経組織(神経ブロック)を作成することに成功した。シリコン製のマイクロチャンバーを用いて神経細胞の生育に最適なサイズ(100-150 um)の神経細胞塊を作成、数日間培養した。その後、取り出した神経細胞塊を培地と共にミリメートルサイズのシリコン製の鋳型(モールド)に入れ培養する事で、巨大な神経ブロックが形成された。神経組織内部では、神経細胞は生体内で観察されるような複雑な形態を有した。さらに神経細胞はミリメートル単位で3次元空間に軸索を伸展、シナプス接続し、3次元神経回路を形成した。また、異なる神経組織領域から取得した神経細胞を利用して作成した神経ブロックを複数個配列する事で、異なる能力域間の3次元神経ネットワークを構築することに成功した。
M. Kato-Negishi, et al.: Advanced Healthcare Materials, 2013.
ニューロスフェロイドによる3次元神経ネットワークの形成
胎児ラットの大脳皮質神経細胞で作られた細胞塊(神経スフェロイド;直径100ミクロン)を利用し、マイクロチャンバー上に人工神経回路を構築する事に成功した。また、この神経回路はチャンバーの特性を生かし、容易に他の物質(ガラス,プラスチック,電極,細胞)に転写可能であり、大脳組織に転写・移植する事も可能だった。移植後、人工神経回路は長期間にわたり機能を有し、さらに脳組織とシナプスを形成する事が確認できた。
M. Kato-Negishi, et al.: Biomaterials, 2010